Nichel, Ni, numero atomico 28
Prezzo, occorrenza, estrazione e uso del nichel
Il nichel è un elemento chimico con l'elemento simbolo Ni e il numero atomico 28. Appartiene ai metalli di transizione, nella tavola periodica si basa sul vecchio metodo di conteggio in 8. Sottogruppo o gruppo ferro-platino, secondo il più recente nel gruppo 10 o gruppo nichel.
Storia
Il nichel fu rappresentato per la prima volta esclusivamente da Axel Frederic Cronstedt 1751 e prende il nome dal minerale cupronickel (kopparnickel svedese, oggi Nickelin) in cui trovò il metallo finora sconosciuto.
I minatori medievali usavano il termine cupronichel per riferirsi al minerale, che sembrava minerale di rame, ma dal quale non si poteva ottenere rame, come se fosse stregato dagli spiriti della montagna ("nichel"). Un'etimologia simile a un coboldo può essere trovata nel cobalto.
La prima moneta di puro nichel fu coniata 1881.
Presenza
Il nichel si presenta nella crosta terrestre con un contenuto di circa il 0,008%. Le prove geofisiche e geochimiche suggeriscono che la maggior parte del nichel si trova sulla Terra e su altri pianeti terrestri nel nucleo, dove forma una lega con ferro e alcuni elementi luminosi. Nel nucleo della Terra, la sua frazione di massa secondo gli ultimi modelli è di circa 5,2%.
Il solido, cioè in forma elementare, il nichel è raro. Finora, solo circa le posizioni 50 per il nichel solido documentato (2018), incluso in Australia, Cina, Canada, Russia e Stati Uniti d'America.
Tradizionalmente, la maggior parte della produzione di nichel proviene da minerali solfidici come pentlandite (circa 34% di nichel), ghiaia magnetica al nichel (pirrotite e agglomerato di pentandite) e alcuni altri minerali di nichel come la millerite (circa 64-65% di nichel) e nichel (circa 44% Nickel) ha vinto. Inoltre, i minerali di nichel lateritici, principalmente di Garnierit, una miscela di Népouit (circa 46% di nichel) e Willemseit (circa 29% di nichel), vengono estratti come materie prime per la produzione di nichel. Complessivamente, ad oggi sono noti alcuni minerali di nichel 200 e alcuni hanno un contenuto di nichel molto più elevato di quelli già menzionati, ma sono molto meno comuni di questi. Ad esempio, la rarissima bunsenite è il minerale con il più alto contenuto di nichel fino al 78,58%. I altrettanto rari minerali Heazlewoodite e Awaruit contengono tra 72 e 73% nichel.
L'estrazione si sta spostando a causa dello sfruttamento dei classici depositi solfidici sempre più verso minerali di nichel lateritici. Tuttavia, questi devono essere faticosamente ottenuti mediante lisciviazione con acido ad alta pressione (lisciviazione con acido inglese ad alta pressione).
Per poter degradare economicamente il nichel, il contenuto di nichel del minerale deve essere almeno 0,5%. Gli eventi più importanti si trovano in Canada (Bacino di Sudbury), Nuova Caledonia, Russia (Norilsk e Kola Peninsula), Australia (Queensland) e Cuba (Moa Bay e Nicaro). Un compagno comune al nichel è il cobalto.
Nichel come minerale

Il nichel naturale nella sua forma elementare è stato descritto per la prima volta da Paul Ramdohr 1967 e riconosciuto dall'International Mineralogical Association (IMA) come specie minerale indipendente (numero di input interno dell'IMA: 1966-039).
Secondo la classificazione dei minerali secondo Strunz (edizione 9) nichel sotto il sistema n. 1.AA.05 (Elementi - Metalli e composti intermetallici - Famiglia rame cupalite - Gruppo rame), rispettivamente, nel obsoleto 8. Edizione elencata sotto I / A.04b (serie nichel). La classificazione dei minerali secondo Dana, che viene utilizzata principalmente nei paesi di lingua inglese, porta l'elemento minerale nel sistema n. 01.01.11.05 (gruppo ferro-nichel).
Il tipo di località è la penisola di Bogotà vicino a Canala nella provincia settentrionale della Nuova Caledonia, dove nichel nativo sotto forma di grani cubi idiomorfi o cubi incarniti a circa 0,1 mm come inclusioni in Heazlewoodite e come una massa irregolare "spidery" trovata tra Heazlewooditkörnern. Minerali di accompagnamento oltre alla Heazlewoodite comprendono calcopirite, calcocite, galena, Godlevskit, rame solido, millerite, orcelite, pentlandite, pirite e pirrotite.
Estrazione e presentazione
La maggior parte del nichel deriva da minerali di ferro contenenti nichel e rame come la ghiaia magnetica al nichel. Al fine di effettuare l'estrazione in modo economico, il nichel deve prima essere arricchito mediante flottazione a circa il cinque percento di contenuto di nichel. Quindi il minerale viene arrostito in modo simile alla produzione di rame. Qui, il minerale viene prima pre-torrefatto per convertire una parte del solfuro di ferro in ossido di ferro. Successivamente, vengono aggiunti silicati e coke per scorie l'ossido di ferro come silicato di ferro. Allo stesso tempo, la pietra grezza rame-nichel è formata da nichel, rame e solfuro di ferro. Poiché questo è specificamente più pesante delle scorie di silicato di ferro, le due fasi possono essere toccate separatamente.
Successivamente, la pietra grezza viene riempita in un convertitore e viene aggiunta la silice. Viene iniettato ossigeno. Di conseguenza, il solfuro di ferro rimanente viene arrostito in ossido di ferro e quindi strofinato. Il risultato è la pietra fine rame-nichel, che comprende circa il 80% di rame e nichel e circa il 20% di zolfo.
| Posizione | Paese | Produzione (in milioni di t) |
|---|---|---|
| 1 | Indonesia | 400.000 |
| 2 | Filippine | 230.000 |
| 3 | Nuova Caledonia | 210.000 |
| 4 | Canada | 210.000 |
| 5 | Australia | 190.000 |
| 6 | Russia | 180.000 |
| 7 | Brasile | 140.000 |
| 8 | Repubblica popolare cinese | 98.000 |
| 9 | Guatemala | 68.000 |
| 10 | Kuba | 51.000 |
Estrazione di Rohnickel
Per recuperare i Rohnickels il nichel deve essere separato dal rame. A tale scopo, la pietra fine viene fusa con solfuro di sodio Na2S. Solo un leggero doppio solfuro di fusione si forma tra rame e solfuro di sodio. Si formano due fasi facili da separare di doppio solfuro di rame-sodio (liquido) e nichel solfuro. Dopo la separazione, il solfuro di nichel viene tostato in ossido di nichel e quindi ridotto in nichel con coke.
Per recuperare il nichel puro, il Rohnickel è raffinato per elettrolisi. A tale scopo, il Rohnickel è collegato come un anodo, un Nickelelfeinblech come un catodo in una cella elettrolitica. L'elettrolita utilizzato è una soluzione di sale di nichel. Durante l'elettrolisi, il nichel e tutti i componenti meno nobili vanno in soluzione nell'anodo. Tutti i componenti più nobili rimangono solidi e cadono sotto l'elettrodo come fango dell'anodo. Questo serve come fonte importante per la produzione di metalli preziosi, come oro o platino. Al catodo, gli ioni di nichel della soluzione sono ridotti a nichel, tutti i componenti meno nobili rimangono in soluzione. La purezza del nichel elettrolitico è intorno allo 99,9%.
Per l'estrazione di nichel puro con una purezza di 99,99% esiste un processo speciale il processo lunare, che prende il nome da Ludwig Moon, che ha scoperto il tetracarbonile di nichel 1890. Questo processo si basa sulla formazione e decomposizione del nichel tetracarbonile. A tal fine, la polvere di Rohnickel finemente suddivisa viene portata in un flusso di monossido di carbonio a 80 ° C. Ciò forma il tetracarbonile di nichel gassoso. Questo viene liberato dalla polvere di scarico e inviato a una camera di decomposizione calda 180 ° C. All'interno ci sono piccole palline di nichel. A questo punto, il nichel tetracarbonile si decompone nuovamente in nichel e monossido di carbonio. Ciò si traduce in nichel molto puro.
la rappresentazione del lavoro
Esistono diversi metodi per rappresentare piccole quantità di nichel molto puro in laboratorio:
Riduzione dell'ossido con idrogeno da 150 ° C a 250 ° C:
Riduzione di una sospensione di cloruro di nichel (II) in dietil etere attraverso una reazione di Grignard
Decomposizione termica di ossalato di nichel (II) in assenza di ossigeno:
Riduzione del cloruro di nichel (II) con una dispersione di sodio:
In particolare, la termolisi dell'ossalato fornisce polvere di nichel piroforico finemente suddivisa.
Proprietà
Proprietà fisiche
Il nichel è un metallo bianco argenteo che è uno dei metalli pesanti con una densità di 8,91 g / cm3. È medio duro (durezza Mohs 3,8), dimenticabile, duttile e può essere lucidato molto bene. Il nichel, come ferro e cobalto, è ferromagnetico, con una temperatura di Curie di 354 ° C. Il metallo si cristallizza in una struttura di cristallo centrata sulla faccia cubica (tipo rame) nel gruppo spaziale Fm3m (numero del gruppo spaziale 225) con il parametro reticolare a = 352,4 pm e quattro unità di formula per unità di cella. Questa struttura lo mantiene anche ad alte pressioni fino ad almeno 70 GPa. Un'altra modifica metastabile con baderna sferica centrata sul corpo cubico potrebbe essere ottenuta in strati sottili su ferro o arsenuro di gallio. Ha una temperatura Curie significativamente più bassa con 183 ° C.
La resistenza alla trazione del nichel ricotto in 400-450 MPa è a un allungamento alla rottura tra 30 e 45%. I valori di durezza sono attorno all'80 HB. Il nichel rinforzato a freddo il cui allungamento alla rottura è inferiore a 2% raggiunge punti di forza fino a 750 MPa con valori di durezza intorno a 180 HB. I semilavorati di nichel puro con contenuto di 99% Ni possono essere rinforzati a freddo.
L'isotopo 62Ni ha la più alta energia di legame per nucleo di tutti gli isotopi di tutti gli elementi.
Proprietà chimiche
Il nichel è molto stabile a temperatura ambiente per aria, acqua, acido cloridrico e alcali. Gli acidi diluiti attaccano il nichel solo molto lentamente. Rispetto agli acidi concentrati e ossidanti (acido nitrico), la passivazione avviene analogamente all'acciaio inossidabile. Il nichel è solubile in acido nitrico diluito (da circa 10 a 15 percento). Anche un acido nitrico semi-concentrato (circa il 30 percento) provoca una passivazione evidente. Lo stato di ossidazione più comune è + II, più raramente si osservano -I, 0, + I, + III e + IV. Nel nichel tetracarbonile, il nichel ha il numero di ossidazione 0. I sali di nichel (II) si dissolvono in acqua per formare complessi acquosi di colore verdastro.
Il nichel finemente suddiviso reagisce con monossido di carbonio da 50 a 80 ° C per formare nichel tetracarbonile, Ni (CO) 4, un liquido incolore, molto tossico. Questo funge da intermedio per la produzione di nichel puro mediante il processo lunare. A 180 a 200 ° C, il tetracarbonile di nichel si decompone in nichel e monossido di carbonio.
Fisiologia
La controversa essenzialità del nichel si contrappone all'esistenza di numerosi enzimi che normalmente contengono nichel, ma non dipendono da esso perché il suo ruolo di catione può essere assunto da altri cationi bivalenti. Nell'uomo, queste sono tre proteine note per legare il nichel:
l'alfa-fetoproteina lega il nichel, ma non dipende da esso, poiché non esiste un enzima
Acireductone dioxygenase, un enzima della via di salvataggio della metionina che lega tipicamente il nichel o un altro catione bivalente
Polibonucleotide 5'-idrossil chinasi Clp1, che richiede come cofattore magnesio, manganese o nichel
Per le piante e vari microrganismi, l'essenzialità del nichel è dovuta all'isolamento di numerosi enzimi (ad es. Ureasi, Co-F430) contenenti nichel nel sito attivo, nonché dal rilevamento di carenze in ambienti poveri di nichel, che sono migliorati dall'aggiunta di Ni (II ) Sali, garantiti.
In elettrofisiologia, gli ioni di nichel sono usati per bloccare i canali del calcio attivati dalla tensione.
Problemi di salute
Il nichel è la causa più comune di allergia da contatto con dermatite da nichel: in Germania, si stima che da 1,9 a 4,5 milioni di persone siano sensibilizzate al nichel. Per questo motivo, i metalli e le leghe che vengono a contatto con la pelle sono sempre meno nichelati. Circa il 10% di tutti i bambini è sensibilizzato al nichel. In caso di rinnovo contatto con l'allergene, possono reagire con un'allergia da contatto.
Secondo l'Autorità europea per la sicurezza alimentare (EFSA), l'assunzione giornaliera tollerabile (TDI) di nichel è di microgrammi 2,8 (0.0028 milligrammi) per chilo di peso corporeo. 2019 ha incaricato la Camera di lavoro dell'Alta Austria di esaminare dodici diverse bevande alla soia presso l'Agenzia per la salute e la sicurezza alimentare. I valori erano tra 0,25 (Dennree drink di soia naturale) e 0,69 milligrammi per litro (sì, ovviamente bevanda di soia biologica). Nel latte di soia più calorico, un chilo 30 di bambini pesanti ha già consumato più del doppio del nichel in un quarto di litro come raccomandato dall'EFSA.
L'inalazione di composti inorganici del nichel è associata ad un aumentato rischio di cancro per carcinoma a cellule squamose del polmone e del tratto respiratorio superiore. Tali neoplasie maligne sono riconosciute come malattie professionali in Germania per esposizione professionale (BK 4109). Inoltre, l'aumento del contenuto di nichel nell'aria e nell'acqua potabile è un fattore di rischio per la sensibilizzazione del nichel nei bambini.
L'uso del nichel nei beni di consumo (come orologi da polso, giocattoli, attrezzature per la lavorazione degli alimenti, ecc.) È limitato dalla normativa dell'Unione Europea, che è stata implementata in Germania dall'ordinanza sui beni di consumo, che stabilisce valori limite per il rilascio.
Utilizzare
Il nichel è necessario come metallo in piccole quantità, la maggior parte della produzione è destinata alla produzione di acciai inossidabili e leghe di nichel. Il nichel viene utilizzato in molti beni industriali e di consumo specifici e identificabili, tra cui acciaio inossidabile, magneti Alnico, monete, batterie ricaricabili, corde di chitarra elettrica, capsule microfoniche, placcature su impianti idraulici e leghe speciali come Permalloy, Elinvar e Invar. È usato per il rivestimento e come tinta per il vetro. Le riserve di depositi di nichel esaurite dal punto di vista odierno sono comprese tra 70 e 170 milioni di tonnellate. Attualmente, oltre un milione di tonnellate (2006: 1,340 milioni di tonnellate) vengono prodotte in tutto il mondo ogni anno. Il prezzo del nichel è talvolta soggetto a oscillazioni di prezzo molto elevate dovute alla speculazione dei mercati finanziari.
Circa il 25 percento del deposito mondiale di nichel si trova in Nuova Caledonia, un territorio francese d'oltremare.

Batteria al nichel cadmio, immagine Wikipedia
Usa come metallo
Il metallo nichel puro viene utilizzato in forma finemente suddivisa come catalizzatore nell'idrogenazione degli acidi grassi insaturi. A causa della sua resistenza chimica, il nichel viene utilizzato per apparecchi nel laboratorio chimico e nell'industria chimica (ad esempio crogioli di nichel per le digestioni). Da nichel metallo leghe di nichel, z. Per le monete.

Filo di nichel (filo), filo di nichel può essere tirato fino a 0,01mm sottile
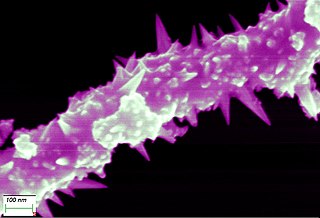
Filo di nichel 0,01mm considerato da un microscopio ad alte prestazioni
Il nichel funge da rivestimento in metallo per la protezione dalla corrosione ("nichelatura") di oggetti metallici: a causa delle sue proprietà protettive contro l'ossidazione, i metalli (in particolare il ferro) sono rivestiti con uno strato di nichel per determinati scopi tecnici mediante la tecnologia galvanica.
Il metallo era anche usato in precedenza per realizzare le montature di occhiali in nichel.
Come emettitore beta, l'isotopo di nichel 63Ni viene utilizzato nei rivelatori di cattura di elettroni nei gascromatografi.
Utilizzare come lega
Il nichel è un importante metallo legato che viene utilizzato principalmente per la finitura dell'acciaio. La maggior parte del nichel va lì. Rende l'acciaio resistente alla corrosione e ne aumenta la durezza, tenacità e duttilità. Gli acciai altolegati con nichel sono utilizzati in ambienti particolarmente corrosivi. L'acciaio inossidabile V2A (il nome deriva dal "test batch 2 austenitic" nelle acciaierie Krupp, corrisponde a X12CrNi18-8) contiene l'8% di nichel oltre al 18% di cromo, V4A (marchi Cromargan o Nirosta) l'11% oltre al 18% di cromo e il 2% di molibdeno.

Monete di nichel foto Wikipedia
Il nichel è un eccellente agente legante per alcuni metalli preziosi e viene utilizzato nella prova del fuoco come collettore di elementi del gruppo del platino. Come tale, il nichel è in grado di raccogliere completamente tutti e sei gli elementi del gruppo del platino, in particolare il platino e il palladio, dai minerali e raccogliere parzialmente l'oro.
Schiuma di nichel o maglia di nichel viene utilizzata negli elettrodi a diffusione di gas per celle a combustibile alcaline.
Il nichel e le sue leghe sono spesso usati come catalizzatori per reazioni di idrogenazione. Il nichel Raney, una lega nichel-alluminio finemente suddivisa, è una forma comune, sebbene vengano utilizzati anche catalizzatori correlati, compresi i catalizzatori di tipo Raney.
Circa il 20% del nichel viene utilizzato (in Germania) per la produzione di altre leghe di nichel:
Konstantan, una lega di 55% rame e 45% nichel, che ha una resistività elettrica approssimativamente costante in un ampio intervallo di temperature. Viene utilizzato principalmente per resistenze accurate.
Le superleghe a base di nichel sono leghe specialmente per l'uso ad alte temperature e sotto fluidi corrosivi. Sono utilizzati, ad esempio, nelle turbine degli aeromobili e nelle turbine a gas delle centrali elettriche.
Raney Nickel, una lega di nichel-alluminio che è un catalizzatore importante per l'idrogenazione dei composti organici.
Argento al nichel, una lega di rame-nichel-zinco con contenuto di nichel 10-26%, che è particolarmente resistente alla corrosione e viene utilizzato principalmente per le posate e le apparecchiature elettrotecniche.
Monel, anche una lega rame-nichel con circa 65% nichel, 33% rame e 2% ferro, che è caratterizzata da una particolare resistenza chimica, incluso il fluoro. Viene quindi utilizzato per bombole di gas di fluoro.
Ghisa sferoidale austenitica, una speciale ghisa sferoidale con nichel fino al 20%, per l'uso in ambienti corrosivi e ad alte temperature.
prova
La reazione di rilevazione per i sali di nichel (II), che di solito sono solubili in acqua di colore verde, viene effettuata gravimetricamente e qualitativamente nella separazione quantitativa con la soluzione dimetilgliossima (reagente di Tschugajew). I sali di nichel sono stati precedentemente facoltativamente precipitati dal solfuro di ammonio sotto forma di solfuro di nichel grigio-nero (II) e disciolti in acido nitrico. La rilevazione specifica è quindi possibile mediante reazione con dimetilgliossima in soluzione ammoniacale. Il bis (dimetilgliossimato) nichel rosso (II) lampone precipita come un complesso:
Poiché il nichel è precipitato quantitativamente dalla soluzione ammoniacale con dimetilgliossima, questa rilevazione è utile anche per l'analisi quantitativa gravimetrica del nichel. Dalla soluzione ammoniacale, si può anche effettuare una determinazione quantitativa mediante elettrogravimetria su un elettrodo a maglia di platino. Simile ad altri metalli pesanti, oggi il nichel è solitamente determinato quantitativamente dalla spettroscopia atomica o dalla spettrometria di massa anche nella regione dell'ultratrace. Estremamente sensibile è la voltammetria inversa con accumulo di adsorbimento del complesso Ni-dimetiglicossima su gocce pendenti di mercurio o film di mercurio.
Connessioni
Il nichel si presenta in composti principalmente nello stato di ossidazione + II. I livelli 0, + I, + III e + IV sono rari e generalmente instabili. Il nichel forma una varietà di complessi per lo più colorati.
Ossido
L'ossido di nichel (II) e l'ossido di nichel (III) sono solidi verdi e neri, rispettivamente, e sono usati per produrre ceramiche, vetri ed elettrodi. Inoltre, vengono utilizzati come catalizzatori per l'idrogenazione di composti organici. Spesso, come molti altri ossidi metallici binari, l'ossido di nichel (II) non è stechiometrico, il che significa che il rapporto nichel-ossigeno si discosta da 1: 1. Questa proprietà è accompagnata da un cambiamento di colore in cui l'ossido di nichel (II) stechiometrico corretto è verde e l'ossido di nichel (II) non stechiometrico è nero. L'ossido di nichel (III) ha un forte effetto ossidante ed è sconosciuto come sostanza pura.
alogenuri
Il cloruro di nichel (II) è un solido giallo, altamente igroscopico, che funge da colorante per la ceramica e per la produzione di catalizzatori di nichel. Oltre alla forma anidra, ci sono ancora cloruri di nichel idrato (II), z. Come il nichel verde (II) cloruro esaidrato, che si è cristallizzato da soluzioni acquose di cloruro di nichel. Il cloruro di nichel anidro (II) ha una struttura cristallina trigonale di tipo cloruro di cadmio (II) avente il gruppo spaziale R3m (gruppo spaziale n. 166). L'esaidrato si cristallizza nel sistema cristallino monoclino nel gruppo spaziale C2 / m (gruppo spaziale n. 12).
Il fluoruro di nichel (II) è anche altamente igroscopico e forma cristalli tetragonali da giallastri a verdi. A differenza di molti fluoruri, è stabile nell'aria. Si cristallizza nel sistema cristallino tetragonale con il gruppo spaziale P42 / mnm (numero del gruppo spaziale 136). Il tetraidrato si cristallizza nel sistema cristallino ortorombico con il gruppo spaziale P21ab (gruppo spaziale numero 29, posizione 3).
Altri composti di nichel inorganici
L'idrossido di nichel (II) e l'ossido di nichel (III) sono utilizzati per immagazzinare energia elettrica nel nichel-cadmio e in altri accumulatori di nichel.
Il nitrato di nichel (II) viene utilizzato nell'industria ceramica come pigmento marrone, nella tintura come mordente, per la nichelatura elettrolitica, per il recupero dell'ossido di nichel (II) e per la produzione di nichel catalizzatore puro. Il nitrato di nichel (II) è un forte ossidante e di solito si presenta sotto forma del suo esa esaidrato Ni (NO3) 2 · 6 H2O.
Nichel (II) solfato e ammonio nichel (II) solfato sono utilizzati nella placcatura (nichelatura). Il solfato di nichel (II) è il composto di nichel tecnicamente più importante. È utilizzato per la produzione di altri composti e catalizzatori di nichel. Le soluzioni acquose di solfato di nichel (II) e cloruro di nichel (II) sono utilizzate per l'elettrodeposizione di strati metallici di nichel. Inoltre, viene utilizzato nella tintura come mordente e nella produzione di maschere antigas.
Il carbonato di nichel (II) si presenta in diverse forme di idrato. È usato come catalizzatore nell'indurimento del grasso e per la produzione di ossido di nichel (II), vernici ceramiche (pigmenti) e smalti e in galvanica. Ha formato un sistema di cristalli trigonali con il gruppo spaziale R3c (numero del gruppo spaziale 161).
Il solfuro di nichel (II) precipita da soluzioni ammoniacali, ma non acide, contenenti nichel con solfuro di ammonio. Di conseguenza, il nichel può essere separato con il gruppo solfuro di ammonio nel processo di separazione cationica.
Il nichel antimonide è un minerale metallico lucido e ha un colore rosso ramato brillante. L'antimonide al nichel viene utilizzato come materiale nelle piastre di campo magnetico dove viene inserito tra gli strati magneticamente sensibili dell'antimonide indio. Le piastre di campo magnetico cambiano la loro resistenza elettrica in funzione della densità del flusso magnetico e fungono da sensore per i campi magnetici. Forma una struttura cristallina esagonale nel gruppo spaziale P63 / mmc (numero del gruppo spaziale 194).
Composti organici di nichel
Nickel tetracarbonyl Ni (CO) 4 è un liquido incolore, molto tossico. È un importante intermedio nel processo lunare. Il tetracarbonile di nichel è stato il primo composto carbonilico di metallo scoperto.
complessi del nichel
Gli ioni di nichel e soprattutto di nichel (II) formano molti complessi per lo più colorati. I numeri di coordinamento 6, 5 o 4 sono i più comuni. Nel caso di ligandi monodentati deboli, ad esempio l'acqua, sono solitamente presenti come complessi ottaedrici e paramagnetici ad alto spin con numero di coordinazione 6. I ligandi forti come il cianuro formano complessi quadrangolari, diamagnetici a basso spin. La dimetilgliossima forma anche un complesso planare quadrato, poiché il complesso è ulteriormente stabilizzato da legami idrogeno. Quest'ultimo complesso bis (dimetilgliossimato) nichel (II) è importante per la rivelazione chimica umida del nichel. I complessi di nichel anionico terminano in "-niccolato".
Esempi di complessi di ammine sono il complesso di nichel blu tetraammina (II) e nichel hexaammina viola (II). Entrambi i composti sono ottenuti aggiungendo ammoniaca a soluzioni saline di nichel (II):
L'aggiunta di cianuro di potassio a soluzioni saline di nichel (II) inizialmente produce cianuro di nichel (II), che si dissolve in eccesso di cianuro di potassio in tetracianoniccolato di potassio giallo (II):
Un composto corrispondente è formato con tiocianato di potassio. Un composto molto sensibile è l'esafluoroniccolato di potassio (IV) (K2 [NiF6]). Il tetracianoniccolato di potassio (II) può essere preparato da nichel monovalente utilizzando un forte agente riducente K4 [Ni2 (CN) 6]. Inoltre, ci sono una varietà di complessi con ligandi organici come etilendiammina o anioni di acidi carbossilici.


![{\ displaystyle {\ ce {NiC2O4 -> [T] [] Ni + 2 CO2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4f5ac7119d30ce593cf99675097e91e39e33a04d)


![{\ displaystyle {\ ce {NiSO4 + 4NH4 + + 4OH- -> [Ni (NH3) 4] SO4 + 4H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/fed711e628c3ba92046eb178a459488074a035c9)
![{\ displaystyle {\ ce {Ni (CN) 2 + 2KCN -> K2 [Ni (CN) 4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7a2b8181f20f5d9ad99c2900689b699739283d0d)
