Ittrio, Y, numero atomico 39
generale
L'ittrio [ʏtriʊm] è un elemento chimico con il simbolo dell'elemento Y e il numero ordinale 39. Appartiene ai metalli di transizione e ai metalli delle terre rare, nella tavola periodica è nell'5. Periodo e 3. Sottogruppo (gruppo 3) o gruppo scandio. L'ittrio prende il nome dal primo sito, la miniera di Ytterby vicino a Stoccolma, nonché Ytterbium, Terbium ed Erbium.
L'ittrio (da Ytterby, il mio vicino alla capitale svedese Stoccolma) è stato scoperto da Johan Gadolin 1794 in Mineral Ytterbit. 1824 ha prodotto Friedrich Wöhler contaminando ittrio riducendo il cloruro di ittrio con potassio. Solo 1842 successe a Carl Gustav Mosander che separava l'ittrio dagli elementi di accompagnamento erbio e terbio.
L'ittrio non si trova in natura nello stato elementare. I minerali contenenti ittrio (Yttererden) sono sempre associati ad altri metalli delle terre rare. Può anche essere contenuto nei minerali di uranio. Le sabbie monazite con fino a 3% ittrio e bastnasite con 0,2% ittrio sono commercialmente degradabili. Inoltre, è il principale costituente dello xenotime (Y [PO4]).
Great Monazitvorkommen, l'inizio dell'19. Scoperti e sfruttati in Brasile e in India nel 20 ° secolo, questi due paesi sono diventati i principali produttori di minerali di ittrio. Solo l'apertura della Mountain Pass Mine in California, che ha prodotto grandi quantità di bastnasite fino agli 1990, ha reso gli USA il principale produttore di ittrio, sebbene il bastnasite estratto lì contenga solo una piccola quantità di ittrio. Dalla chiusura di questa miniera, la Cina è il più grande produttore di terre rare dell'60%. Questi sono ottenuti in una miniera vicino a Bayan Kuang, il cui minerale contiene xenotime, e da minerali argillosi ad assorbimento ionico, che vengono estratti principalmente nella Cina meridionale.

Ittrio metallo
recupero
La separazione delle terre rare l'una dall'altra è un passo laborioso nella produzione di ittrio. La cristallizzazione frazionata di soluzioni saline era il metodo preferito all'inizio, che è stato utilizzato all'inizio per la separazione su scala di laboratorio delle terre rare. Solo l'introduzione della cromatografia ionica ha permesso di separare le terre rare su scala industriale.
L'ossido di ittrio concentrato viene convertito in fluoruro. La successiva riduzione al metallo si verifica con il calcio nel forno ad induzione sotto vuoto.
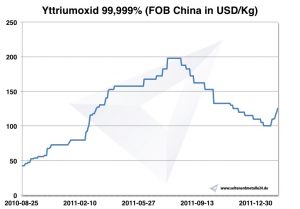
Grafico ossido di ittrio 2010-2011
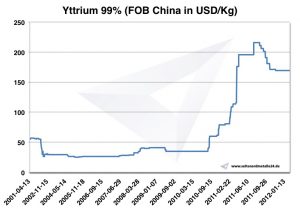
Grafico Ittrio 2001-2012
Particolaritá
L'ittrio è relativamente stabile nell'aria, ma si oscura alla luce. A temperature superiori a 400 ° C, le nuove interfacce potrebbero accendersi. L'ittrio finemente diviso è relativamente instabile. L'ittrio ha una sezione trasversale di cattura bassa per i neutroni.
Nei suoi composti è prevalentemente trivalente. Tuttavia, ci sono anche composti a grappolo in cui l'ittrio può assumere stati di ossidazione <3.
Esistono un totale di isotopi 32 tra 76Y e 108Y, così come altri isomeri del nucleo 24 conosciuti. Di questi, solo uno 89Y, di cui esiste esclusivamente ittrio naturale, è stabile. L'ittrio è uno degli elementi puri di 22. I radioisotopi più stabili sono 88Y con un'emivita di 106,65 giorni e 91Y con un'emivita di 58,51 giorni. Tutti gli altri isotopi hanno un'emivita inferiore a un giorno, ad eccezione di 87Y, che ha un'emivita di 79,8 ore e 90Y con 64 ore. Gli isotopi di ittrio sono tra i prodotti più comuni della fissione dell'uranio nei reattori nucleari e nelle esplosioni nucleari.
Tavola periodica di ittrio-39
Utilizzare
L'ittrio metallico viene utilizzato nella tecnologia dei reattori a tubi. Una lega di ittrio-cobalto può essere utilizzata come magnete permanente. L'ittrio viene utilizzato come materiale per il riscaldamento di fili in sorgenti ioniche di spettrometri di massa. Nella metallurgia, gli additivi di ittrio minori vengono utilizzati per la raffinazione del grano, ad esempio nelle leghe conduttrici di calore ferro-cromo-alluminio, cromo, molibdeno, titanio e leghe di zirconio. Nelle leghe di alluminio e magnesio ha un effetto rinforzante. Tecnicamente più importanti sono i composti ossidici di ittrio:
Nitrato di ittrio come materiale di rivestimento in un mantello
Il granato di alluminio di ittrio (YAG) funge da cristallo laser
Granato di ferro di ittrio (YIG) come filtro a microonde
Zirconio stabilizzato con ittrio come elettrolita solido nelle celle a combustibile (SOFC, cella a combustibile a ossido solido)
Tuttavia, l'uso più importante di ossidi di ittrio e ossidi di ittrio solfuri è la versatilità nei fosfori (fosfori) trivalenti di europio (rosso) e di tulio (blu) in tubi di immagini televisive, lampade fluorescenti e tubi radar.
Inoltre, la ceramica e le leghe di ittrio sono utilizzate in:
sonde Lambda
Superconduttori (ad es. Ossido di ittrio-bario-rame YBa2Cu3O7-x)
leghe ODS
scintilla
Come un puro emettitore beta 90Yttrium è usato in medicina nucleare per la terapia, ad esempio il Radiosynoviorthese.
L'ittrio è considerato non essenziale e tossico (valore MAK = 5 mg / m3).
| Generale | ||
| Nome, simbolo
ordinale |
Ittrio, Y, 39 | |
| Serie | I metalli di transizione | |
| Gruppo, periodo, blocco | 3, 5, d | |
| Aspetto | bianco argenteo | |
| numero CAS | 7440-65-5 | |
| Frazione di massa dell'involucro della terra | 26 ppm | |
| nucleare | ||
| massa atomica | 88,90585 u | |
| raggio atomico | 180 pm | |
| Raggio covalente | 190 pm | |
| Elektronenkonf. | [Kr] 4d (1) 5s2 | |
| 1. ionizzazione | 600 KJ / mol | |
| 2. ionizzazione | 1180 KJ / mol | |
| 3. ionizzazione | 1980 KJ / mol | |
| fisicamente | ||
| stato fisico | fisso | |
| struttura cristallina | esagonale | |
| densità | 4,472 g / cm3 | |
| magnetismo | paramagnetico (χm = 1,2 * 10 (-4)) | |
| punto di fusione | 1799 K (1526 C) | |
| punto di ebollizione | 3609 K (3336 C) | |
| Volume molare | 19,88 * 10 (-6) m (3) / mol | |
| Calore di vaporizzazione | 380 KJ / mol | |
| calore di fusione | 11,4 KJ / mol | |
| Conducibilità elettrica | 1,66 * 10 (6) A / (V * m) | |
| conducibilità termica | 17 W / (m * K) | |
