Bismuto, Bi, numero atomico 83
Bismuto - Storia, occorrenza, estrazione, usi e prezzi del bismuto
Il bismuto o bismuto (anche obsoleto: bismuto) è un elemento chimico con l'elemento simbolo Bi e il numero atomico 83. Nella tavola periodica è in 5. Gruppo principale o gruppo azoto.
Non è noto alcun isotopo stabile. Tuttavia, l'emivita estremamente bassa estremamente bassa radioattività dell'209Bi naturale è irrilevante per l'uso pratico. La radioattività poteva essere rilevata solo su 2003, poiché in precedenza non erano disponibili i metodi altamente sensibili necessari per la misurazione; 1990Bi è stato considerato il nuclide stabile più pesante negli anni 209.
Storia
Come elemento separato, il bismuto divenne il centro di 18. Secolo dai chimici Claude Francois Geoffroy, Johann Heinrich Pott, Carl Wilhelm Scheele e Torbern Olof Bergman hanno dimostrato. In precedenza, veniva spesso considerato un derivato di piombo, stagno, antimonio e altri metalli o minerali. Nel libro Un utile libro di montagna (su 1527), il minerale di Bismuth (wissmad arzcz) è menzionato come compagno del minerale d'argento. Più tardi in 16. Century Georgius Agricola ha provato una distinzione più precisa.
Il nome del metallo, che appare come wesemut in tedesco 1390 e lat. 1450 come wismutum, 1530 come bisemutum, può essere tradotto nella traduzione araba di Dioscuri dell'9. Century è stata attribuita la forma documentata b [i] sīmūtīyūn, che è probabilmente una traslitterazione del greco antico representsιμύθιον psimýthion, lead white 'rappresenta. Fu anche adottata la genesi dell'arabo iṯmid, antimonio; Spesso, oltre al presunto primo ammutinamento nella miniera di San Giorgio nei prati vicino Schneeberg nell'Erzgebirge in 15. Secolo, o sulla variante wis (se) mat. che significa "massa bianca".
Il simbolo chimico Bi è stato suggerito da JJ Berzelius nell'anno 1814.
Presenza
Il bismuto si presenta naturalmente in natura, cioè in forma elementare, ed è riconosciuto come minerale dall'International Mineralogical Association (IMA). 9 utilizzato dall'IMA. L'edizione della classificazione dei minerali dopo Karl Hugo Strunz porta il bismuto insieme all'antimonio, all'arsenico e allo stibarsen nella suddivisione degli elementi di arsenico secondo il sistema n. 1.CA.05 (edizione 8 obsoleta: I / B.01-40). Nella classificazione prevalentemente di lingua inglese dei minerali secondo Dana Bismuth appartiene al "gruppo arsenico" con il sistema n. 01.03.01.
Il bismuto solido si forma in vene idrotermali di pegmatiti e vene di quarzo stagno-tungsteno contenenti topazio e di solito insieme a vari minerali di rame, nichel, argento e stagno. Il bismuto sviluppa raramente forme cristalline ben formate, ma può raggiungere dimensioni fino a 12 centimetri. Di solito si trova sotto forma di aggregati dendritici, laminari o granulari, ma anche come gemelli polisintetici con striature parallele ("bismuto di primavera") o superfici laterali a forma di imbuto disegnate nel centro del cristallo.
(Come 2011) Finora, circa 1400 località di bismuto dignitose sono considerati nota. I siti sono principalmente in Australia, Bolivia, Cina, Canada, Messico, Perù e Spagna, storicamente Bieber in Spessart e in Erzgebirge, dove di bismuto (sia in forma pura e come solfuro (bismutinite) seleniuro (Selenidbismutglanz) e ossido è trovato bismite). Inoltre, il bismuto, così come l'antimonio e l'arsenico, si presenta occasionalmente come doppio solfuro: galenobismuthite (PbBi2S4), lillianite (Pb3Bi2S6), bismuto d'argento (AgBiS2) CuXiXNUMB (XBXXUM) è anche noto un solfuro tellurio in forma di Tellurbismut (Bi2Te6S) e un silicato di nome Eulytin (Bi2 (SiO6) 2).
Complessivamente, sono noti anche solidi bismuti attorno ai minerali di bismuto 230.
Estrazione e presentazione
Per la produzione di bismuto si possono assumere minerali ossidici o solfidici.
I minerali di ossido sono ridotti a bismuto nelle fornaci a carbone:
I sali di bismuto di solfuro possono essere ridotti con il ferro con il metodo delle precipitazioni:
Oppure i minerali solfidici vengono prima convertiti in ossidi e quindi ridotti con carbone (metodo di riduzione di Röder):
Il bismuto grezzo viene quindi rimosso ossidando la fusione di altri elementi (antimonio, arsenico, piombo, ferro e zolfo). Il rame viene rimosso fondendosi con solfuro di sodio, oro e argento mediante estrazione di bismuto fuso con stagno.
Proprietà
Proprietà fisiche
Il bismuto è un metallo bianco-argento, fragile e grossolanamente cristallino o semi-metallo con un tocco di rosa. Ha una struttura cristallina romboedrica con strati doppi molto densi. La distanza più breve tra due doppi strati è 352,9 pm, che è solo 15% maggiore della distanza più piccola tra due atomi all'interno di un doppio strato. I monocristalli di bismuto mostrano una spaccatura pronunciata parallela a questi doppi strati.
Il bismuto ha il più forte effetto Hall di tutti gli elementi simili al metallo e come un semi-metallo in forma pura, una scarsa conducibilità elettrica. Mostra - a parte i superconduttori e la grafite pirolitica - oltre la più forte proprietà diamagnetica, viene espulso da un campo magnetico applicato esternamente. L'effetto Schubnikow-de-Haas (oscillazioni della resistenza elettrica in un campo magnetico esterno) è stato inizialmente osservato sui cristalli di bismuto e misurato. Prima dello sviluppo dei sensori Hall e delle piastre di campo, per misurare i campi magnetici veniva utilizzata la cosiddetta spirale del bismuto, una bobina con filo di bismuto isolato sottile avvolto. Il cambiamento di resistenza della bobina sotto l'influenza di un campo magnetico mutevole era certamente molto piccolo rispetto ai sensori di oggi.
Esistono due modifiche note del bismuto: il bismuto, che è comune a temperatura ambiente, forma una struttura di cristallo cubica centrata sul corpo ad alta pressione (a partire da 9 GPa).
Il bismuto liquido si espande come una delle poche sostanze quando si solidifica (anomalia della densità). Questo fenomeno si osserva anche in gallio, germanio, plutonio, silicio, tellurio e acqua. È basato sul bismuto che durante la fusione (e la solidificazione) ha luogo una transizione a doppia fase: una volta che la transizione di fase 1. Ordine da solido a liquido (di solito con una piccola diminuzione della densità) e in aggiunta una transizione di fase 1. Ordine del metalloide su metallo con significativo aumento della densità, che spiega anche l'entropia insolitamente grande della fusione di 21,1 J / (K · mol) e l'improvviso aumento della conduttività elettrica del fuso di bismuto.
Proprietà chimiche
Il bismuto è resistente all'aria secca a temperatura normale. Nell'aria umida, tuttavia, sulla superficie si forma uno strato di ossido. Inoltre, il bismuto è resistente all'acqua e agli acidi non ossidanti (acido cloridrico e acido solforico diluito). Negli acidi ossidanti (acido nitrico o acido solforico concentrato caldo) il bismuto viene sciolto per formare sali di bismuto (BiX3). In forma di polvere, è un solido infiammabile, può essere facilmente infiammato dalla breve esposizione a una fonte di accensione e continua a bruciare dopo la rimozione. Il rischio di ignizione è maggiore, maggiore è la distribuzione della sostanza. Il metallo in una forma compatta non è infiammabile.
Quando è rovente, il bismuto brucia con una fiamma bluastra in un fumo marrone-giallo - ossido di bismuto (III) (Bi2O3).
Sotto calore il bismuto si combina direttamente con gli alogeni e direttamente con zolfo, selenio e tellurio. Il bismuto non reagisce con azoto e fosforo.
isotopo
Il bismuto naturale è costituito solo dall'isotopo 209Bi. In 2003, l'Institut d'astrophysique spatiale di Orsay (Francia) ha scoperto che questo isotopo, che era stato stabile fino ad ora, è un emettitore alfa con un'emivita di (1,9 ± 0,2) 1019 anni (circa 19 trilioni di anni). Il decadimento molto lento di 209Bi in 205Tl si basa da un lato dalla vicinanza immediata al doppio magico 208Pb nello schema isotopico e dal fatto che 209Bi stesso sia semplicemente magico. La lunga emivita si traduce in un'attività di 0,0033 Bq / kg (corrispondente a un singolo decadimento nucleare per cinque minuti e chilogrammi).
209Bi è il penultimo membro della serie Neptunium e tranne 205Tl l'unico che è ancora naturale. Poiché i nuclidi che sono all'inizio della serie Neptunium vengono ora incubati nei reattori nucleari, la quantità di 209Bi sulla Terra sta aumentando nel tempo.
Utilizzare
Il bismuto è utilizzato come componente di lega in leghe a basso punto di fusione, ad esempio per il metallo di Wood, che fonde a 70 ° C, per il metallo di Rose con un punto di fusione di 98 ° C e per il metallo di Lipowitz, che fonde a 60 ° C.
Uso tecnico
La lega di bismanolo con manganese è un potente magnete permanente.
Nelle leghe di rivestimento (stagnatura a caldo) per connettori solari serve come sostituto del piombo.
Singoli cristalli di bismuto sintetico con dimensioni superiori a centimetri 20 e piastre di bismuto policristallino sono utilizzati come filtri a neutroni per le indagini sui materiali sui reattori di ricerca.
Il tellururo di bismuto composto chimico pompa l'energia termica in elementi Peltier.
Il materiale a cambiamento di fase di alcuni DVD-RAM contiene bismuto, vedi Tecnologia a cambiamento di fase.
Il bismuto viene propagato da alcune fonti come elemento legante negli acciai a taglio libero per sostituire il piombo. Dovrebbe migliorare la lavorabilità di questi acciai senza le proprietà ecologiche negative del piombo. Dal punto di vista della metallurgia dell'acciaio, tuttavia, ciò è sfavorevole, dal momento che il bismuto praticamente non può essere rimosso metallurgicamente e quindi appare come un indesiderato elemento di accompagnamento negli acciai prodotti da rottami. Nel settore elettronico, una lega di stagno di bismuto viene utilizzata come sostituto (parola chiave RoHS) per le saldature al piombo. Lo svantaggio è che per Bismuth è necessaria la propria attrezzatura di saldatura. La contaminazione con piombo (ad es. Riparazione di vecchie apparecchiature) provoca un punto di fusione molto basso, mentre l'uso di utensili in lega di stagno-argento porta a temperature elevate e alla contaminazione dello strumento a bismuto.
L'ossido di bismuto viene utilizzato per la produzione di vetri ottici e per la sinterizzazione di ceramiche tecniche. Trova anche applicazione sotto forma di germanato di bismuto come rivelatore a scintillazione nella tomografia ad emissione di positroni (PET).
Una lega di bismuto di piombo fu usata nell'Unione Sovietica come refrigerante per i reattori nucleari. Sebbene sia più efficace del tradizionale raffreddamento ad acqua in pressione, questa lega è anche più difficile da gestire. La lega si solidifica a una temperatura inferiore a 125 ° C e può quindi causare gravi danni al reattore. Tali reattori sono stati utilizzati, tra l'altro, su sottomarini nucleari (ad esempio sottomarini classe Alfa).
Il bismuto è anche usato come sostituto di piombo non tossico per le munizioni per fucili a pompa. Tuttavia, questo non è molto comune.
In 16. Century fu sviluppato nella Germania meridionale e in Svizzera una tecnica pittorica in cui il bismuto veniva usato come rivestimento per scatole decorative o scatole più piccole, in parte anche per altari di legno. Questa tecnica si chiama pittura di bismuto.
Utilizzare nell'industria chimica
L'ossido di bismuto cloruro (BiOCl) è usato come cosmetico perlato bianco-argento nei cosmetici.
Il vanadio di bismuto è usato come pigmento giallo verdastro altamente resistente agli agenti atmosferici in uso e trova z. B. in vernici di alta qualità, vernici a emulsione per facciate, plastica e inchiostri da stampa.
Inoltre, il bismuto viene utilizzato come catalizzatore nell'industria chimica.
Uso medicinale
Composti di bismuto come il dibismuto tris (tetraossodialuminato), nitrato di bismuto (subnitrato di bismuto, nitrato di bismuto di base) sono usati come parte di una terapia antibiotica contro l'uso del patogeno Helicobacter pylori, che può causare ulcere allo stomaco e duodeno (terapia di eradicazione). L'applicazione è una cosiddetta terapia quadrupla (terapia di combinazione di un inibitore della pompa protonica e una tripla terapia di bismuto [sale di bismuto, tetraciclina, metronidazolo).
I composti di bismuto sono anche parzialmente utilizzati nella diarrea come astringenti e per la riduzione degli odori in alitosi e flatulenza. Inoltre, alcuni composti (ad esempio Bibrocathol) sono usati come antisettici.
Inoltre, il bismuto viene utilizzato in modo diagnostico nella tomografia a emissione di positroni sotto forma di germanato di bismuto come materiale rivelatore dell'apparato tomografico.
Storicamente, il bismuto era alla fine di 19. Secolo come parte delle polveri ferite (ad es. Dermatol) utilizzate. Dagli anni 1920, è stato usato come rimedio per la sifilide. Tuttavia, è stato completamente sostituito da moderni antibiotici.
I sali di bismuto sono stati utilizzati anche come agenti di contrasto dei raggi X per visualizzare il tratto gastrointestinale (il cosiddetto pasto di bismuto). Qui, il sale di bismuto è stato sostituito dal solfato di bario.
Il gallato di bismuto viene utilizzato in una formulazione di salve di pelle Stolte e l'unguento può essere usato per trattare la pelle infiammatoria nei neonati.
Vergiftung
L'avvelenamento da bismuto (bismutismo) è raro a causa del cattivo assorbimento nel tratto gastrointestinale. È in gran parte simile all'avvelenamento da mercurio. Tipico è il verificarsi di un bismuto grigio ardesia (deposizione di solfuro di bismuto) sulla mucosa orale con formazione di mucosa orale (stomatite) e gengivite (con perdita dei denti, perdita), enterite intestinale con diarrea e danno renale (nefropatia del bismuto).
prova
Il bismuto viene rilevato dallo scivolo del bismuto con la tiourea. Il fluoruro di sodio, il cloruro di sodio e il tartrato di sodio e di potassio sono usati per precipitare gli ioni interferenti indesiderati:
NaF per la complessazione di Fe3 + e Al3 +
NaCl per la precipitazione di Ag + e Hg22 +
Tartrato per la complessazione di Sb3 + e Sn2 +
In presenza di Bi3 +, si forma un complesso di tiourea giallo limone giallo, in cui tre molecole di tiourea sono associate al bismuto attraverso lo zolfo:
![{\displaystyle {\ce {\rm {Bi^{3+}{+}3SCN2H4{->}[Bi(SCN2H4)3]^{3+}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c283de06adc520701a39cebdb2d9f9e206572f68)
Reazioni di rilevazione alternative:
In una reazione redox con ioni di stagno (II) come agente riducente, il bismuto elementare fa precipitare il nero.
Con soluzione di ioduro di sodio: prima precipita lo ioduro di bismuto nero (III), che si dissolve in eccesso di ioduro come complesso di tetraiodobismutato di arancio:
![{\ displaystyle {\ ce {\ rm {Bi ^ {3 +} {+} 4I ^ {-} {->} [BiI4] ^ {-}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8f1a3e20448941130afb1ebcb56f6ed3bd093dad)
1,3,4-thiadiazole-2,5-dithiol è adatto anche come agente complessante per il rilevamento.
Connessioni
Il bismuto è principalmente trivalente, ma esiste anche un solo e pentavalente bismuto; Tuttavia, l'ossido di bismuto (V) è un agente ossidante molto forte che ossida persino il manganese (II) per permanganato. Inoltre forma cationi polimerici. È stabile nell'aria.
- composti ossigenati
Ossido di bismuto (III) (bismuto, chiamato anche feci di bismuto) - composti dello zolfo
Bismuto (III) solfuro - composti di idrogeno
Bismuto idrogeno (bismuthan) - Alogenuri e nitrati
Fluoruri: fluoruro di bismuto (III), fluoruro di bismuto (V), fluoruro di ossido di bismuto
Cloruri: cloridrato di bismuto, cloruro di bismuto (III), ossido di cloruro di bismuto
Bromuri: subbromide di bismuto, bromuro di bismuto (III), bromuro di ossido di bismuto
Ioduri: ioduro di bismuto (I), ioduro di bismuto (III), ioduro di ossido di bismuto
Nitrati: nitrato di ossido di bismuto (subnitrato di bismuto) - Come un anione
bismutato sodio (V)
Prezzi, grafici, cronologia dei prezzi
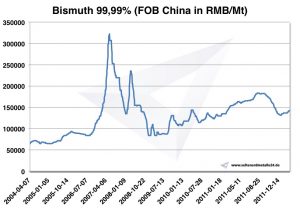
Grafico Bismuto 2004 2011



