Samarium, Sm, numero atomico 62
generale
Il samario (dopo il minerale Samarskit, che a sua volta prende il nome dall'ingegnere minerario WM Samarski) è un elemento chimico con l'elemento simbolo Sm e il numero atomico 62. Nella tavola periodica, l'elemento brillante argenteo appartiene al gruppo dei lantanidi e quindi appartiene anche ai metalli delle terre rare.
Per la scoperta del Samarium, ci sono diverse rappresentazioni in letteratura.
1. 1853 ha mostrato spettroscopicamente il samario svizzero Jean Charles Galissard de Marignac con una linea di assorbimento tagliente nel Didymoxid. 1879 ha isolato il francese Paul Emile Lecoq de Boisbaudran l'elemento del minerale Samarskit (Y, Ce, U, Fe) 3 (Nb, Ta, Ti) 5O16). La designazione di minerali ed elementi deriva dall'ispettore russo delle miniere colonnello Samarsky, che ha scoperto il minerale.
2. 1878 ha scoperto il chimico svizzero Marc Delafontaine Samarium, che chiama Decipum, in ossido di didimio. 1879 scopre in modo indipendente Paul Emile Lecoq de Boisbaudran Samarium. 1881 mostra a Delafontaine che il suo elemento isolato contiene un altro elemento oltre al samario.
3. La scoperta spettroscopica 1 di Marignac su 1853, menzionata sotto 1878, è stata fatta da XNUMX da Paul Emile Lecoq de Boisbaudran.
1903, il chimico tedesco Wilhelm Muthmann ha prodotto samario metallico per elettrolisi.
Certo, il samarium elementare non si verifica. Tuttavia, alcuni minerali come monazite, bastnasite e samarskite contengono l'elemento. La monazite contiene fino al 1% samario.
recupero
A partire dalla monazite o dalla bastnaesite, ha luogo la separazione delle terre rare tramite scambio ionico, estrazione con solvente o deposizione elettrochimica. In una fase finale del processo, l'ossido di samario di elevata purezza con lantanio metallico viene ridotto al metallo e sublimato.
Particolaritá
Il samario è ragionevolmente stabile nell'aria, forma uno strato di ossido giallastro passivante. Il samario metallico scintillante si infiamma a temperature superiori a 150 ° C. Reagisce con l'ossigeno per formare il sesquiossido Sm2O3. Reagisce violentemente con l'acqua per formare idrogeno e idrossido di samario. Come con tutti i lantanoidi, lo stato di ossidazione più stabile è +3. Il samario è disponibile in tre modifiche. I punti di transizione sono 734 ° C e 922 ° C. I cationi Sm3 + ingialliscono le soluzioni acquose.
Esistono quattro isotopi radioattivi stabili e instabili 19. Gli isotopi naturali più comuni sono 152Sm (26,7%), 154Sm (22,7%) e 147Sm (15%).
Utilizzare
Insieme ad altre terre rare per lampade ad arco in carbonio per sistemi di proiezione cinematografica.
Doping di singoli cristalli di fluoruro di calcio per maser e laser.
A causa della sua grande sezione trasversale di neutroni termici ed epitermici, il samario viene utilizzato come assorbitore di neutroni nelle applicazioni nucleari.
Magneti al cobalto di samario:
I magneti permanenti SmCo5 hanno un'elevata resistenza alla smagnetizzazione e una forza coercitiva fino a 2200 kA / m. La lega Sm2Co17 migliorata è più costosa da produrre, ma ha proprietà magnetiche più elevate e una migliore resistenza alla corrosione.
Sono utilizzati nei motori passo-passo per orologi al quarzo, motori di azionamento in dispositivi a nastro in miniatura (walkman, dittafoni), cuffie, sensori, accoppiamenti in agitatori e unità a disco rigido. Come materiali magnetici per il risparmio di peso, vengono utilizzati anche in applicazioni aerospaziali.
L'ossido di samario viene aggiunto al vetro ottico per l'assorbimento della luce infrarossa.
I composti del samario sono usati per sensibilizzare il fosforo (fosforo) quando irradiato con luce infrarossa.
Come catalizzatore; L'ossido di samario catalizza l'idrogenazione e la deidrogenazione dell'etanolo (alcool).
In medicina, l'isotopo 153Samarium viene utilizzato in associazione con un bisfosfonato (Lexidronam) per il trattamento del dolore osseo nei tumori (terapia con radionuclidi per metastasi ossee).
I composti con samario nello stato di ossidazione meno favorevole + 2 (in particolare samario (II) ioduro e samario (II) bromuro) trovano applicazione nella sintesi organica (agente riducente e reagente di trasferimento di un elettrone, ad es. Accoppiamenti pinacol mediati da samario) ,
In associazione con l'etilendiamminetetra radiofarmaceutica (acido metilenfosfonico) in medicina nucleare per il trattamento palliativo delle metastasi ossee e scheletriche.
| Generale | |
| Nome, simbolo
ordinale |
Samarium, Sm, 62 |
| Serie | lantanidi |
| Gruppo, periodo, blocco | La, 6, f |
| Aspetto | bianco argenteo |
| numero CAS | 7440-19-9 |
| Frazione di massa dell'involucro della terra | 6 ppm |
| nucleare | |
| massa atomica | 150,36 u |
| raggio atomico | 185 pm |
| Raggio covalente | 198 pm |
| Elektronenkonf. | [Xe] 4f (6) 6s2 |
| 1. ionizzazione | 544,5 KJ / mol |
| 2. ionizzazione | 1070 KJ / mol |
| 3. ionizzazione | 2260 KJ / mol |
| fisicamente | |
| stato fisico | fisso |
| struttura cristallina | trigonal |
| densità | 7,536 g / cm3 (25 ° C) |
| magnetismo | paramagnetico (χm = 1,12 * 10 (-3)) |
| punto di fusione | 1345 K (1072 C) |
| punto di ebollizione | 2076 K (1803 C) |
| Volume molare | 19,98 * 10 (-6) m (3) / mol |
| Calore di vaporizzazione | 175 KJ / mol |
| calore di fusione | 8,6 KJ / mol |
| Conducibilità elettrica | 1,06 * 10 (6) A / (V * m) |
| conducibilità termica | 13 W / (m * K) |
Prezzi del samario
Prezzi del samario -> prezzi delle terre rare
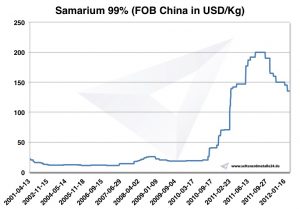
Grafico Samarium 2001-2012
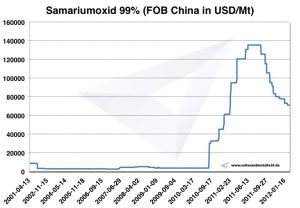
Grafico Ossido di samario 2001-2012