Tungsteno, W, numero atomico 74
Prezzo del tungsteno, occorrenza, estrazione e uso
Il tungsteno [vɔlfram] è un elemento chimico con il simbolo dell'elemento W e il numero atomico 74. Appartiene ai metalli di transizione, nella tavola periodica è in 6. Sottogruppo (gruppo 6) o gruppo cromo. Il tungsteno è un metallo pesante bianco lucido ad alta densità che è fragile allo stato puro. Ha il punto di fusione più alto e il secondo punto di ebollizione più alto di tutti i metalli puri. Il suo uso più noto è quindi il filamento incandescente nelle lampade a incandescenza.
Già in 16. Il mineralogista Georgius Agricola di Freiberger ha descritto la presenza di un minerale nei minerali di stagno sassone, che ha reso l'estrazione di stagno tagliando la frazione di stagno considerevolmente più difficile. Il nome componente "Wolf" deriva da questa proprietà, poiché il minerale "divorava" il minerale di stagno come un lupo. Se fosse tungstenite è ancora controverso oggi, poiché parla della "leggerezza" del minerale. Ha chiamato il minerale lupi spumumche tradotto dal latino significa "schiuma di lupo". Successivamente è stato chiamato Wolfram, da mhd. Ariete "Fuliggine, sporcizia", perché il minerale grigio-nero può essere facilmente macinato e quindi ricorda la fuliggine. Il suo simbolo chimico W deriva dal tungsteno.
La parola comune in inglese, italiano e francese Tungsteno deriva da Tung Sten (Svedese per "pietra pesante"). Ciò non significava che Wolfram stesso (svedese Volfram), ma chiamato tungstato di calcio. In questo 1781 ha riconosciuto al chimico tedesco-svedese Carl Wilhelm Scheele un sale finora sconosciuto. Il tungsteno puro è stato prodotto per la prima volta da 1783 dai fratelli spagnoli Fausto Juan José Elhuyar (che lavorava sotto la guida di Scheele) riducendo il triossido di tungsteno, ottenuto dal wolframite.
Presenza

Il metallo tungsteno chiamato anche wolframite
Il contenuto di tungsteno della crosta terrestre è di circa 0,0001 g / to 0,0064 percento in peso (valore di Clarke). Finora, il metallo non è stato rilevato in natura (in forma pura). La "Doklady Akademii Nauk" in Russia ha pubblicato un rapporto sul tungsteno solido nel 1995 senza che questo fosse esaminato dalla "Commissione sui nuovi minerali, nomenclatura e classificazione" (CNMNC) dell'IMA. Sono noti alcuni minerali, soprattutto ossidi e tungstati. I minerali di tungsteno più importanti sono la wolframite (Mn, Fe) WO4 e Scheelite CaWO4, Esistono anche altri minerali di tungsteno, come Stolzit PbWO4 e Tuneptit WO3 · H2O.
I depositi più grandi si trovano in Cina, Perù, Stati Uniti, Corea, Bolivia, Kazakistan, Russia, Austria e Portogallo. I minerali di tungsteno si possono trovare anche nei Monti Metalliferi. I depositi mondiali sicuri e probabili sono attualmente 2,9 milioni di tonnellate di tungsteno puro.
La più importante presenza nota di tungsteno in Europa è nella Felbertal negli Alti Tauri (stato di Salisburgo in Austria).
Promozione in tutto il mondo
Nel 2006 la produzione mondiale di tungsteno puro è stata di 73.300 tonnellate. Di gran lunga il più grande produttore di tungsteno è la Cina. Più dell'80% del tungsteno prodotto nel mondo viene prodotto lì. Gli stati con la più alta produzione di tungsteno (2006):
| Posizione | Paese | Tariffe di consegna (in tonnellate all'anno) |
|---|---|---|
| 1 | Cina | 62.000 |
| 2 | Föd russo. | 4.500 |
| 3 | Canada | 2.500 |
| 4 | Austria | 1.350 |
| 5 | Portogallo | 900 |
| 6 | Corea del Nord | 600 |
| 7 | Bolivia | 530 |
| 8 | altri paesi | 900 |
Promozione in Austria
In Austria, il minerale di tungsteno Scheelite fu scoperto per la prima volta nel 1815/16 nel giacimento d'oro di Schellgaden nel comune di Muhr (Stato di Salisburgo). Di conseguenza, in molte fessure degli Alti Tauri sono stati trovati bellissimi cristalli di scheelite, a volte di diversi centimetri di dimensione. Tutti questi reperti non erano di alcuna utilità pratica. Il grande giacimento nella Felbertal non è stato scoperto per il momento.
Nel 1950 si è saputo che grandi quantità di scheelite erano apparse nel giacimento di magnesite sulla Wanglalm vicino a Lanersbach / Tux (Tirolo) nella parte posteriore della Zillertal, che era stata estratta dal 1927. Era una grossolana scheelite ricoperta di magnesite e quarzo. Negli anni successivi sono state estratte circa 10.000 tonnellate di minerale con un contenuto medio di ossido di tungsteno dell'1,8%, che rappresentava un'alta qualità unica al mondo. A causa del basso prezzo di mercato, l'estrazione del tungsteno fu interrotta alla fine degli anni '1960, ma riprese nel 1971 e continuò fino alla chiusura della miniera di magnesite nel 1976.
1967 alla fine è stato scoperto il più grande Scheelitvorkommen in Europa nel Felbertal. I pezzi di minerale presenti nei flussi sono stati tracciati utilizzando la luce UV (fluorescenti di Scheelite). Il difficile lavoro di esplorazione in alta montagna (il sito minerario più alto di Brentling in 2100 a livello del mare) iniziò 1971, l'estrazione inizialmente in superficie fu registrata in Felbertal 1976 (da 1979 anche miniere sotterranee, set di miniere 1986). Dall'inizio di 1993 alla metà di 1995, il mining è stato temporaneamente sospeso a causa del basso prezzo di mercato del tungsteno.
Wolframerz del Felbertal viene processato nel vicino Mittersill. Da qui, il concentrato di scheelite raggiunge Sankt Martin in Sulmtal (Stiria). Una capanna di tungsteno è stata costruita sul sito della miniera sotterranea di carbone marrone 1976 a Pölfing-Bergla, dove ossido di tungsteno, metallo di tungsteno e polvere di carburo di tungsteno sono stati prodotti da concentrati provenienti da diversi paesi da 1977.
I processori tedeschi più importanti sono HC Starck e il Longyear GmbH.
Estrazione e presentazione
Il tungsteno non può essere ottenuto per riduzione con carbone dai minerali di ossido, poiché si forma questo carburo di tungsteno.
L'aggiunta di una soluzione ammoniacale crea un complesso chiamato paratungstato di ammonio (APW). Questo viene filtrato e quindi convertito in triossido di tungsteno relativamente puro a 600 ° C. Ossido di tungsteno (VI) (WO3), che viene ridotto a tungsteno grigio acciaio a 800 ° C in atmosfera di idrogeno:
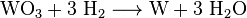
Questo produce polvere di tungsteno grigia, che di solito viene compattata in stampi e sinterizzata elettricamente in barre. A temperature superiori a 3400 ° C, un metallo compatto di tungsteno può essere fuso in speciali forni elettrici con atmosfera riducente di idrogeno (processo di fusione a zone).
Proprietà
Proprietà fisiche
Il tungsteno è un metallo bianco lucido che può essere allungato allo stato puro ed è di elevata durezza, densità e resistenza. La densità è quasi la stessa di quella dell'oro, la durezza Brinell è 250 HB, la resistenza alla trazione 550-620 N / mm2 (morbido) fino a 1920 N / mm2 (difficile). Il metallo esiste in una modifica α cubica centrata sul corpo stabile con una spaziatura del piano reticolare (= costante reticolare) di 316 pm a temperatura ambiente. Questo tipo di struttura cristallina è spesso chiamato tipo di tungsteno. Con un as β-modifica metastabile di tungsteno (distorto centrato sul corpo cubico), d'altra parte, è l'ossido ricco di tungsteno W3O.
Il tungsteno ha dopo l'elemento carbonio con 3422 ° C il secondo punto di fusione più alto di tutti gli elementi chimici. Il punto di ebollizione di 5555 ° C è superato solo dal raro renio metallico con 5596 ° C di 41 K.
Il metallo è un superconduttore con una temperatura di transizione di 15 mK.
Proprietà chimiche
Il tungsteno è un metallo chimicamente molto resistente che viene difficilmente attaccato da acido fluoridrico e aqua regia (almeno a temperatura ambiente). Si dissolve in miscele di acidi fluoridrico e nitrico e miscele fuse di nitrati alcalini e carbonati.
isotopo
Il tungsteno è noto come isotopi 33 e isomeri del nucleo 5. In natura, si verificano isotopi 5 180W, 182W, 183W, 184W e 186W. L'isotopo di tungsteno 184W ha la frequenza maggiore. Tutti e 5 gli isotopi naturali sono stati considerati stabili per molto tempo. È solo nel 2004 che l'esperimento CRESST dei Laboratori nazionali del Gran Sasso riesce a dimostrare che l'isotopo era un risultato secondario della ricerca della materia oscura 180W è soggetto a decadimento alfa. L'emivita è estremamente lunga 1,8 trilioni di anni, quindi questo decadimento non può essere rilevato in un normale ambiente di laboratorio. La radioattività di questo isotopo naturale è così bassa che può essere ignorata per tutti gli scopi pratici. Al contrario, gli isotopi radioattivi artificiali del tungsteno hanno una breve emivita compresa tra 0,9 ms 185Giorni W e 121,2 a 181W.
Utilizzare
L'applicazione più importante del tungsteno è dovuta al suo elevato punto di fusione nel settore dell'illuminazione come filamento nelle lampade a incandescenza e come elettrodo nelle lampade a scarica di gas e nei tubi elettronici.
Nelle lampadine si fa uso del fatto che la conduttività elettrica del tungsteno è notevolmente inferiore a quella dei metalli conduttivi rame e alluminio. Di conseguenza, il sottile filamento di tungsteno si riscalda fino a quando non si illumina, mentre i conduttori più spessi dei metalli conduttivi difficilmente si riscaldano.
La sua seconda importanza principale come metallo legante nella metallurgia del ferro. Forma carburi di tungsteno negli acciai per utensili che aumentano la durezza secondaria.
Grazie alla sua alta densità, è usato per bilanciare pesi e proteggere le radiazioni. Sebbene la sua densità, e quindi l'effetto di schermatura, sia molto più elevato di quello del piombo, è meno comunemente usato come piombo per questo scopo perché è più costoso e più difficile da elaborare. Inoltre, a causa dell'alta densità del tungsteno in alcuni eserciti, le munizioni perforanti vengono utilizzate con un nucleo di proiettile in carburo di tungsteno invece dell'uranio più economico ma radioattivo e tossico. Nella seconda guerra mondiale Wolfram fu importante per la costruzione della granata di carri armati tedesca 40, che aveva un nucleo di tungsteno. In futuro, le munizioni con nucleo di tungsteno del nuovo veicolo di fanteria corazzato Puma verranno utilizzate per sostituire la martora.
A causa della sua elevata resistenza alla corrosione, il tungsteno può essere utilizzato anche come materiale per apparecchiature in impianti chimici. Tuttavia, a causa della scarsa lavorabilità del tungsteno (il tungsteno può essere saldato solo mediante laser o fascio di elettroni), questa forma di realizzazione viene utilizzata raramente. Lo stesso vale per un'applicazione concepibile nel campo della tecnologia medica.
In fisiologia, in particolare la neurofisiologia, i microelettrodi di tungsteno sono utilizzati per le registrazioni extracellulari.
Inoltre, gli elettrodi per i processi di saldatura sono fabbricati in tungsteno. Ad esempio, nella saldatura a resistenza, specialmente quando si saldano materiali come rame, bronzo o ottone. Anche nella saldatura universale TIG (Tungsten Inert Gas), un elettrodo è realizzato in tungsteno o una sua lega. Questi elettrodi non si sciolgono durante il processo di saldatura. L'arco brucia come plasma in un gas protettivo tra l'elettrodo e il componente. Il materiale di riempimento viene fornito separatamente sotto forma di barre.
Negli sport Wolfram viene utilizzato per la produzione di botti di alta qualità per le freccette, nelle punte da tiro con l'arco per frecce speciali sono state realizzate e le teste a martello sono state temporaneamente prodotte per ridurre la resistenza dell'aria e il raggio di rotazione anche in tungsteno. Inoltre, le lastre di tungsteno vengono utilizzate come pesi aggiuntivi nella formula 1 per raggiungere il peso minimo prescritto delle vetture 1 Formula (inclusi olio, freni e liquido di raffreddamento, nonché i conducenti in tuta da corsa e con casco) di 620 kg (a partire da: 2010). Anche nella vela arriva da tempo nelle bombe a chiglia dei grandi piloti utilizzati. La resistenza all'acqua è notevolmente ridotta dalla maggiore densità rispetto ai materiali convenzionali come piombo o ghisa. Allo stesso modo, ci sono già delinquenti nel tennis, nel cui telaio sono state incorporate fibre di tungsteno in fibra di carbonio. In questo modo è possibile stabilizzare ulteriormente aree specifiche del telaio della racchetta per aumentare la precisione del gioco.
Nella pesca a mosca, ninfe e stelle filanti (esche pescate sott'acqua) vengono appesantite con palline di tungsteno che vengono forate e spinte sul gambo dell'amo, in modo che si immergano più velocemente e più in profondità.
Le corde per strumenti musicali a volte vengono avvolte con tungsteno per aumentarne il peso e quindi ridurre il tono.
Il tungsteno viene anche utilizzato nella diagnostica a raggi X come materiale target nell'anodo. Il  - e
- e  Le linee di radiazione a raggi X caratteristiche sono 59 keV e 67 keV.
Le linee di radiazione a raggi X caratteristiche sono 59 keV e 67 keV.
Nella microscopia a tunneling a scansione, il tungsteno viene spesso utilizzato come materiale per la punta della sonda.
Dall'inizio di 21. Il carburo di tungsteno, erroneamente indicato come tungsteno, viene utilizzato anche in gioielleria (gioielli in tungsteno), ad es. B. anelli elaborati. Questo è molto facilmente determinato dalla durezza e dalla densità. WC ha la durezza Mohs 9,5, solo tungsteno 7,5. Finora, tutte le parti di gioielleria sul mercato sono realizzate in carburo di tungsteno.
Fisiologia
Il tungsteno è considerato un bioelemento positivo di batteri anaerobici del tipo Eubacterium acidaminophilum usato e incorporato come cofattore in alcuni enzimi. E. acidaminofilo è un batterio che fermenta gli amminoacidi che utilizza il tungsteno negli enzimi formiato deidrogenasi e aldeide deidrogenasi. In questi organismi, il tungsteno sostituisce il molibdeno perché è molto più comune nel loro ambiente naturale (prese d'aria vulcaniche sul fondo del mare).
tossicologia
Secondo le attuali conoscenze, il tungsteno e i suoi composti sono fisiologicamente innocui. I tumori polmonari nei lavoratori negli impianti di produzione o lavorazione del carburo cementato sono attribuiti al cobalto che è anche presente.
Nel modello animale è stato riscontrato che la maggior quantità di composti di tungsteno ingeriti per via orale viene rapidamente escreta nelle urine. Una piccola parte del tungsteno entra nel plasma sanguigno e da lì negli eritrociti. Viene quindi depositato nei reni e nel sistema osseo. Tre mesi dopo la somministrazione, la maggior parte delle piccolissime quantità di tungsteno assorbite dal corpo si trovano nelle ossa.
2003 è stato identificato con 16 in 1997 con XNUMX in bambini affetti da leucemia e con nove bambini anche con tumore del sangue in Sierra Vista / Arizona, due cosiddetti ammassi di cancro - un'area locale con un tasso di cancro superiore alla media. In entrambi i luoghi, l'acqua potabile ha concentrazioni insolitamente elevate di tungsteno. Concentrazioni di tungsteno significativamente aumentate sono state rilevate nelle urine della popolazione. Entrambi i luoghi sono noti per la loro presenza di minerali di tungsteno. Tuttavia, nessuna associazione diretta tra le malattie di tungsteno e leucemia è stata trovata nelle successive indagini di un anno da parte del Center for Disease Control (CDC). Il tungsteno non ha mostrato alcun effetto cancerogeno in nessuna procedura di test e nessun altro gruppo di tumori è stato trovato in altre parti del Nevada con livelli simili di tungsteno nelle urine della popolazione.
sicurezza
Come polvere o polvere, è facilmente infiammabile, non infiammabile in forma compatta.
Connessioni
Ossido
Il tungsteno forma diversi ossidi. Tra il membro iniziale:
- Ossido di tungsteno (VI) WO3 - giallo limone
e l'ultimo membro:
- Ossido di tungsteno (IV) WO2 - marrone
Ci sono altri ossidi intermedi?
- W10O29 blu-viola, gamma di omogeneità WO2,92-DOVE2,88
- W4O11 rosso-viola, gamma di omogeneità WO2,76-DOVE2,73
- W18O49, DOVE2,72
- W20O50, DOVE2,50
Altri composti
- Sodio tungstato Na2WO4
- Tungstato di zirconio ZrW2O8 mostra un'anomalia quando riscaldato.
- Bronzi al tungsteno MxWO3; M = metallo alcalino, metallo alcalino terroso, lantanoide, circa 0.3 <x <0.9 hanno conducibilità elettrica e sono intensi e di colore diverso a seconda del contenuto di metallo.
- Calcio tungstato CaWO4 è conosciuto come un minerale sotto il nome di Scheelite.
- Il carburo di tungsteno WC è un composto simile al metallo estremamente duro. C'è anche Diwungsten Carbide W.2C.
- Esafluoruro di tungsteno WF6
- Piombo tungstato PbWO4
- Disolfuro di tungsteno WS2 Utilizzare come lubrificante secco (simile a MoS2)
Uso dei composti
Il carburo di tungsteno viene utilizzato come riflettore di neutroni nelle armi nucleari per ridurre la massa critica. I carburi di tungsteno (metallo duro) vengono utilizzati nella lavorazione dei materiali a causa della loro elevata durezza.
I tungstati vengono utilizzati per impregnare i tessuti per renderli ignifughi.
I colori al tungsteno sono usati nella pittura, nell'industria della ceramica e della porcellana.
Il tungstato di piombo è usato come un moderno scintillatore nella fisica delle particelle.
| Generale | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nome, simbolo, numero atomico | Tungsteno, W, 74 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serie | I metalli di transizione | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppo, periodo, blocco | 6, 6, d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspetto | bianco grigiastro, lucido | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| numero CAS | 7440-33-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Frazione di massa del guscio di terra | 64 ppm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| nucleare | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| massa atomica | 183,84 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raggio atomico (calcolato) | 135 (193) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raggio covalente | 162 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| configurazione elettronica | [Xe] 4f145d46s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. ionizzazione | 770 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. ionizzazione | 1700 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| fisicamente | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| stato fisico | fisso | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| struttura cristallina | cubico centrato sul corpo | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| densità | 19,3 g / cm3 (20 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| durezza Mohs | 7,5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| magnetismo | paramagnetico ( = 7,8 10-5) = 7,8 10-5) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto di fusione | 3695 K (3422 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto di ebollizione | 5828 K (5555 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volume molare | 9,47 · 10-6 m3/ mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calore di vaporizzazione | 824 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| calore di fusione | 35,4 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| velocità del suono | 5174 m/s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacità termica specifica | 138 J / (kg · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conducibilità elettrica | 18,52 · 106 A / (V · m) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| conducibilità termica | 170 W / (m · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chimico | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| stati di ossidazione | 6, 5, 4, 3, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| potenziale normale | −0,119 V (WO2 + 4H+ + 4e- → W + 2H2O) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| elettronegatività | 2,36 (scala Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| isotopo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| proprietà NMR | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| sicurezza | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
Frasi H e P di pericolo H: 228EUH: nessuna tariffa EUHP: 210-240-241-280-370+378 Gefahrstoffkennzeichnung
 |
| leggero infiammabile |
| (F) |
Frasi R e S in polvere R: 11S: 43
Prezzo al tungsteno
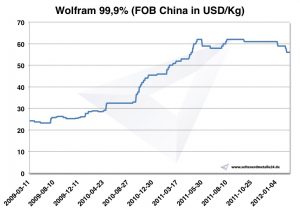
Grafico Wolfram 2009-2012
