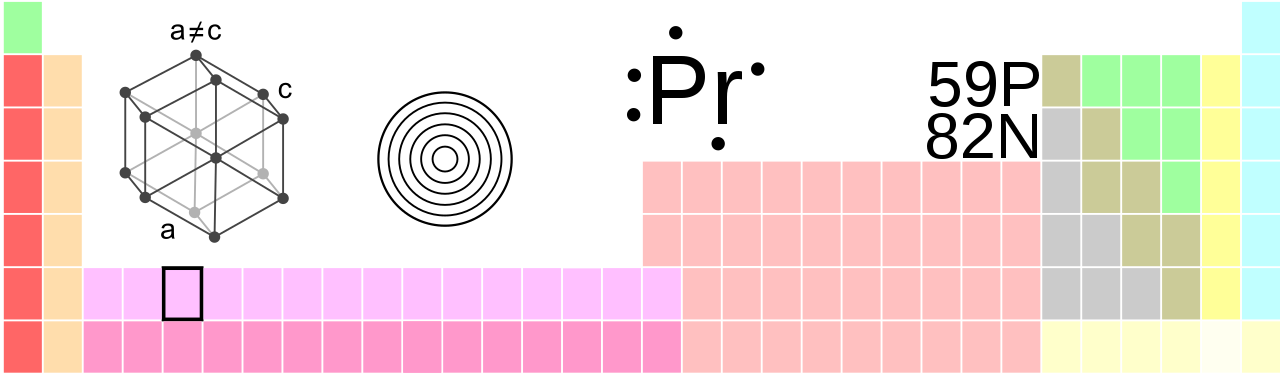
Praseodimio, Pr, numero atomico 59
generale
Il praseodimio è un elemento chimico con l'elemento simbolo Pr e il numero atomico 59. Nella tavola periodica appartiene al gruppo dei lantanidi e quindi appartiene anche ai metalli delle terre rare. Dal colore verde dei suoi composti deriva il nome: la parola greca prásinos significa "porro verde", didimo "doppio" o "gemello".
1841 Carl Gustav Mosander estrasse il raro Didym di terra dall'ossido di lantanio. 1874 ha osservato a Per Teodor Cleve che Didym era in realtà due elementi. Nell'anno 1879 Lecoq de Boisbaudran samarium isolato da Didym, che ha vinto dal minerale Samarskit. 1885 è riuscito a separare Carl Auer von Welsbach, Didym in Praseodimio e Neodimio, che formano entrambi i sali di diversi colori.
Il praseodimio è un compagno nei tipici minerali delle terre rare Cerit, Monazit e Bastnäsit. Le riserve mondiali sono stimate in 4 milioni di tonnellate.
recupero
Come per tutti i lantanidi, i minerali vengono prima arricchiti dalla flottazione, quindi i metalli vengono convertiti in alogenuri corrispondenti e separati da cristallizzazione frazionata, scambio ionico o estrazione. Il metallo è ottenuto mediante elettrolisi del sale fuso o riduzione del calcio.
Particolaritá
Il praseodimio è un morbido metallo paramagnetico bianco-argento, che appartiene ai lantanidi e ai metalli delle terre rare. È un po 'più resistente alla corrosione nell'aria rispetto all'europio, al lantanio o al cerio, ma forma facilmente uno strato di ossido verde che si sfalda nell'aria. A 798 ° C, l'α-Pr esagonale si converte nel β-Pr cubico centrato sul corpo. Il praseodimio naturale è costituito solo dall'isotopo stabile 141Pr. Sono noti altri 38 isotopi radioattivi, di cui 143Pr e 142Pr sono i più longevi, con emivite rispettivamente di 13,57 giorni e 19,12 ore. Tutti gli altri isotopi hanno un'emivita inferiore a 5,985 ore e la maggior parte anche inferiore a 33 secondi. Ci sono anche 6 stati metastabili, con 138mPr (t½ 2,12 ore), 142mPr (t½ 14,6 minuti) e 134mPr (t½ 11 minuti) che sono i più stabili.
Gli isotopi hanno una gamma di massa atomica da 120,955 (121Pr) a 158,955 (159Pr). A causa della sua sensibilità all'aria, il praseodimio deve essere conservato sotto benzina o sigillato in plastica o vetro.
Non è noto un significato biologico, ma si dice che i composti del praseodimio siano leggermente dannosi per il fegato. Tuttavia, non ci sono valori di tossicità.
Il praseodimio si presenta nei suoi composti trivalente e tetravalente, con il numero di ossidazione trivalente che è il più abbondante. Gli ioni Pr (III) sono di colore giallo-verde e gli ioni Pr (IV) sono incolori. In particolari condizioni riduttive e praseodimio bivalente possono essere realizzati, per. Ad esempio in Pr2I5.
Sono noti diversi alogenuri di tutti gli stadi, ad esempio PrF3, PrF4, PrCl3, PrBr3, PrI3, Pr2I5. Gli alogenuri trivalenti formano idrati diversi.
Esistono anche vari composti con calcogeni: il normale praseodimio marrone-nero (III, IV) ossido Pr6O11, il PrO2 quasi nero, il Pr2O3 verde, Pr2S3, Pr2Te3 e altri composti binari come PrN, PrP. Inoltre, il praseodimio è presente in vari sali, come il nitrato di praseodimio igroscopico Pr (NO3) 3.xH2O, il praseodimosolfato splendidamente cristallizzante Pr2 (SO4) 2.8 H2O e altri.
Inoltre, forma diversi complessi di fluorido come tali. Ad esempio, il K2 [PrF6] con Pr quadrivalente.
Utilizzare
Il praseodimio viene utilizzato in leghe con magnesio per la produzione di metallo ad alta resistenza per motori aeronautici.
Il cobalto e le leghe di ferro sono potenti magneti permanenti.
I composti del praseodimio vengono utilizzati per colorare vetri e smalti (ad esempio nelle lenti dei proiettori di colore verde nella tecnologia di illuminazione).
I composti migliorano anche l'assorbimento dei raggi UV e vengono utilizzati per occhiali protettivi per gli occhi durante la saldatura.
| Generale | |
| Nome, simbolo
ordinale |
Praseodimio, Pr, 59 |
| Serie | lantanidi |
| Gruppo, periodo, blocco | La, 6, f |
| Aspetto | bianco argenteo, giallastro |
| numero CAS | 7440-10-0 |
| Frazione di massa dell'involucro della terra | 5,2 ppm |
| nucleare | |
| massa atomica | 140,90765 u |
| raggio atomico | 185 pm |
| Raggio covalente | 203 pm |
| Elektronenkonf. | [Xe] 4f (3) 6s2 |
| 1. ionizzazione | 527,0 KJ / mol |
| 2. ionizzazione | 1020 KJ / mol |
| 3. ionizzazione | 2086 KJ / mol |
| fisicamente | |
| stato fisico | fisso |
| struttura cristallina | esagonale |
| densità | 6,475 g / cm3 (25 ° C) |
| magnetismo | paramagnetico (χm = 2,9 * 10 (-3)) |
| punto di fusione | 1208 K (935 C) |
| punto di ebollizione | 3563 K (3290 C) |
| Volume molare | 20,80 * 10 (-6) m (3) / mol |
| Calore di vaporizzazione | 330 KJ / mol |
| calore di fusione | 6,9 KJ / mol |
| Conducibilità elettrica | 1,43 * 10 (6) A / (V * m) |
| conducibilità termica | 13 W / (m * K) |
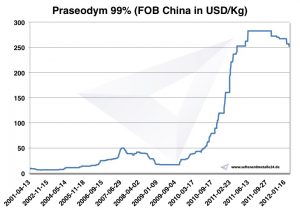
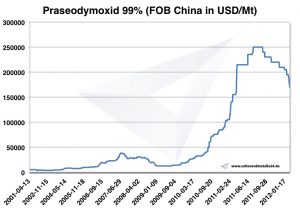
Prezzo del praseodimio
Prezzi del praseodimio -> prezzi delle terre rare