Lantanio, La, numero atomico 57
generale
Il lantanio [lantaːn] è un elemento chimico con il simbolo dell'elemento La e il numero atomico 57. Appartiene ai metalli di transizione e ai metalli delle terre rare, nella tavola periodica si trova lo 6. Periodo e 3. Sottogruppo (gruppo 3) o gruppo scandio. Principalmente viene anche contato dal Lanthanoiden, anche se la f-shell dell'elemento non è occupata.
Lantanio (greco λανθάνειν, lanthanein, "da nascondere") 1839 è stato scoperto dal chimico e chirurgo svedese Carl Gustav Mosander. Da un presunto nitrato di cerio puro vinse per cristallizzazione frazionata Lanthanum sulfate.
Il lantanio si trova naturalmente solo nei composti chimici associati ad altri lantanidi in vari minerali. Principalmente questi sono:
Monazite ((Ce, La, Th, Nd, Y) PO4)
Bastnäsit ((Ce, La, Y) CO3F)
recupero
Dopo una complessa separazione dell'altro compagno di lantanide, l'ossido viene fatto reagire con fluoruro di idrogeno in fluoruro di lantanio. Successivamente, questo viene ridotto a lantanio con calcio per formare fluoruro di calcio. La separazione dei residui di calcio rimanenti e delle impurità avviene in un'ulteriore rifusione sotto vuoto.
Particolaritá
Il metallo bianco argenteo è malleabile e duttile. Vi sono tre modifiche metalliche.
Il lantanio non è dignitoso. Viene rapidamente rivestito con uno strato di ossido bianco nell'aria, che reagisce nell'aria umida all'idrossido.
A temperature superiori a 440 ° C il lantanio brucia in ossido di lantanio (La2O3). La formazione di idrogeno in acqua fredda è lenta, in acqua calda una rapida reazione all'idrossido. Negli acidi diluiti, il lantanio si dissolve sotto evoluzione dell'idrogeno. Con molti elementi reagisce direttamente nel calore, con alogeni anche a temperatura ambiente. Lantanio e idrogeno formano un idruro non stechiometrico nero sensibile all'acqua.
Utilizzare
Il lantanio è un componente in metallo misch. I materiali di silice piroforica contengono da 25 a 45 percentuale in peso di lantanio. Inoltre, trova impiego come agente riducente nella metallurgia. Come aggiunta di ghisa, supporta la formazione di grafite sferoidale, come additivo legante, migliora la resistenza all'ossidazione. Le miscele di lantanio riducono la durezza e la sensibilità alla temperatura del molibdeno.
I catodi di alta qualità per la generazione di elettroni liberi sono costituiti da esaboruro di lantanio in sostituzione del filo di tungsteno. L'ossido di lantanio ad alta purezza viene utilizzato nell'industria del vetro per la produzione di vetri di alta qualità con un indice di rifrazione elevato per l'ottica z. B. utilizzato per obiettivi fotografici.
Con Cobalto:
La lega di cobalto-lantanio LaCo5 viene utilizzata come materiale magnetico, titanato di bario drogato con lantanio per la produzione di termistori PTC (resistori dipendenti dalla temperatura). In combinazione con cobalto, ferro, manganese, stronzio e altri, funge da catodo per celle a combustibile ad alta temperatura (SOFC). Il nichel di lantanio "contaminato" (LaNi5) viene utilizzato come accumulo di idrogeno nelle batterie di accumulo di idruro di nichel metallico. Inoltre, è disponibile nelle lampade ad arco in carbonio per l'illuminazione da studio e nei sistemi di proiezione cinematografica (applicazione storica?) Prima.
Con titanio:
Un metallo in lega con composizioni materiali di lantanio e titanio, l'effetto è attribuito al fatto che con la lavorazione a truciolo, la lunghezza del truciolo è ridotta. Ciò dovrebbe facilitare la lavorazione del metallo.
Nel campo della medicina, gli strumenti resistenti alla corrosione e facilmente sterilizzabili sono prodotti dal metallo legato. Si dice che questa lega metallica a base di titanio sia particolarmente adatta per strumenti e apparecchi chirurgici poiché la propensione all'allergia nell'uso di tale lega metallica con titanio rispetto ad altre leghe dovrebbe essere bassa.
Come ossido di lantanio
Produzione di occhiali (Lanthanglas) con indice di rifrazione relativamente elevato, che a sua volta cambia solo leggermente con la lunghezza d'onda (bassa dispersione), per macchine fotografiche, obiettivi per telescopi e per occhiali
Produzione di cristalli e macchie di porcellana. Sostituisce i composti di piombo più tossici con il miglioramento simultaneo della resistenza chimica (miglioramento della resistenza agli alcali, "lavabile in lavastoviglie")
Aggiunta di catalizzatore alle zeoliti durante il cracking catalitico fluido nella raffineria di petrolio
Produzione di masse ceramiche a condensatore e vetri privi di silicati
Componente di lucidatrici per vetro
Produzione di catodi caldi per tubi di elettroni (anche boruri di lantanio)
Come carbonato di lantanio
Farmaco per abbassare il livello di fosfato nei pazienti in dialisi (cosiddetto legante fosfato)
Il lantanio è classificato come a bassa tossicità. Una dose tossica non è nota. Tuttavia, la polvere di lantanio è considerata altamente corrosiva perché reagisce molto facilmente, ad esempio con l'umidità della pelle, all'idrossido di lantanio basico (simile agli elementi calcio e stronzio). La dose letale nei ratti è 720 mg.
| Generale | |
| Nome, simbolo Numero ordine | Lantanio, La, 57 |
| Serie | I metalli di transizione |
| Gruppo, periodo, blocco | 3, 6, d |
| Aspetto | bianco argenteo |
| numero CAS | 7439-91-0 |
| Frazione di massa dell'involucro della terra | 17 ppm |
| nucleare | |
| massa atomica | 138,9055 u |
| raggio atomico | 195 pm |
| Raggio covalente | 207 pm |
| Elektronenkonf. | [Xe] 5d (1) 6s2 |
| 1. ionizzazione | 538,1 KJ / mol |
| 2. ionizzazione | 1067 KJ / mol |
| 3. ionizzazione | 1850 KJ / mol |
| fisicamente | |
| stato fisico | fisso |
| struttura cristallina | esagonale |
| densità | 6,17 g / cm3 (20 ° C) |
| magnetismo | paramagnetico (χm = 5,4 * 10 (-5)) |
| punto di fusione | 1193 K (920 C) |
| punto di ebollizione | 3743 K (3470 C) |
| Volume molare | 22,39 * 10 (-6) m (3) / mol |
| Calore di vaporizzazione | 400 KJ / mol |
| calore di fusione | 6,2 KJ / mol |
| Conducibilità elettrica | 1,626 * 10 (6) A / (V * m) |
| conducibilità termica | 13 W / (m * K) |
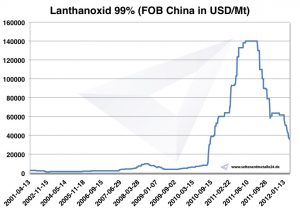
Prezzo del lantanio